Артериальное давление при коарктация аорты

Медицинский эксперт статьи
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Коарктация аорты – это ограниченное сужение просвета аорты, которое приводит к гипертензии сосудов верхних конечностей, гипертрофии левого желудочка и гипоперфузии органов брюшной полости и нижних конечностей. Симптомы коарктации аорты варьируют в зависимости от степени сужения и его протяженности – от головной боли, боли в области грудной клетки, холодных конечностей, слабости и хромоты до фульминантной сердечной недостаточности и шока. Мягкий шум можно услышать над местом сужения. Диагноз ставят на основании эхокардиографии или КТ или МР-ангиографии. Лечение коарктации аорты – баллонная ангиопластика со стентированием или хирургическая коррекция. Рекомендуется проводить профилактику эндокардита.
Коарктация аорты составляет 8-10 % среди всех врожденных пороков сердца. Она отмечается у 10-20 % пациентов с синдромом Шерешевского-Тернера. Соотношение мальчиков и девочек составляет 2:1.
Коарктация аорты обычно развивается в проксимальном отделе грудной аорты непосредственно под местом отхождения подключичной артерии. Редко происходит коарктация брюшной аорты. Коарктация может быть изолированным пороком либо сочетаться с другими врожденными аномалиями (например, бикуспидальный клапан аорты, дефект межжелудочковой перегородки, стеноз аорты, открытый артериальный проток, аномалии митрального клапана, аневризмы головного мозга).
Физиологические последствия включают увеличение нагрузки давлением на левый желудочек, гипертрофию левого желудочка, гиперперфузию верхней половины тела, в том числе головной мозг, и гипоперфузию органов брюшной полости и нижних конечностей.
[1], [2], [3], [4], [5], [6], [7], [8]
Симптомы коарктации аорты
Возможно два варианта коарктации аорты:
- изолированная коарктация (взрослый тип);
- коарктация аорты в сочетании с открытым артериальным протоком, сужение аорты при этом расположено пре- или постдуктально (детский тип).
Детский тип коарктации наиболее неблагоприятен, так как он сопровождается очень ранним формированием высокой лёгочной гипертензии. Сужение аорты преграждает кровоток из сердца к органам нижней половины тела, вследствие чего возрастает артериальное давление выше места сужения. Это приводит к формированию особенностей телосложения – «атлетического» телосложения с хорошо развитым плечевым поясом, а также к появлению жалоб, характерных для артериальной гипертензии (головные боли, носовые кровотечения). При естественном течении порока могут развиться морфологические изменения коронарных артерий, вторичный фиброэластоз эндо- и миокарда левого желудочка, расстройства мозгового кровообращения или кровоизлияния в мозг, что также ухудшает результаты отложенного хирургического лечения.
При значительном сужении в периоде новорожденности могут развиться циркуляторный шок с почечной недостаточностью (олигурия или анурия) и метаболический ацидоз, напоминая клинику других системных заболеваний, например сепсиса.
Менее выраженное сужение может не проявляться клинически на первом году жизни. Неспецифические симптомы коарктации аорты (например, головная боль; боль в области грудной клетки, слабость и хромота при физических нагрузках) могут появляться по мере роста ребенка. Часто отмечается гипертензия, однако сердечная недостаточность редко развивается после периода новорожденности. Редко происходит разрыв аневризмы головного мозга, что приводит к субарахноидальному или внутричерепному кровоизлиянию.
Типичными результатами при физикальном обследовании являются гипертензия сосудов верхних конечностей. Пульс на бедренной артерии слабый или отстающий, низкое или не определяемое АД на нижних конечностях. Систолический шум изгнания интенсивности 2-3/6 лучше всего выслушивается в межлопаточной области слева. Расширенные межреберные коллатеральные артерии могут приводить к появлению продолжительного шума в межреберных пространствах. У девочек с коарктацией аорты может отмечаться синдром Тернера, врожденное заболевание, при котором развиваются лимфатические отеки ног, крыловидные складки на шее, квадратная грудная клетка, cubitus valgus, широко расставленные соски.
При отсутствии лечения во взрослом возрасте может развиться левожелудочковая сердечная недостаточность, разрыв аорты, внутричерепное кровоизлияние, гипертензионная энцефалопатия и гипертоническая болезнь.
Диагностика коарктации аорты
Диагноз предполагают на основании клинических данных (включая измерение АД на всех 4 конечностях), с учетом рентгенографии органов грудной клетки и ЭКГ, точный диагноз устанавливают на основании двухмерной эхокардиографии с цветной допплеркардиографией или КТ или МР-ангиографии.
Клиническая диагностика коарктации аорты специфична, характерные симптомы обращают на себя внимания уже при первом осмотре. Область сердца визуально не изменена. Границы относительной сердечной тупости не расширены. Выслушивается интенсивный систолический шум на основании сердца, точка максимального выслушивания – между лопатками на уровне второго грудного позвонка. Пульс на бедренной артерии ослаблен или не пальпируется. артериальное давление на ногах значительно снижено или не определяется. Если порок впервые выявляют в возрасте старше 1 года, это свидетельствует о его относительно малой выраженности. Выраженная коарктация аорты проявляется уже в первые месяцы жизни беспокойством, плохой прибавкой в весе, отсутствием аппетита. Поскольку измерение артериального давления у грудных детей затруднено, при обследовании обязательно определяют пульс на бедренных артериях и оценивают его характеристики.
На ЭКГ обычно отмечается гипертрофия левого желудочка, однако ЭКГ может быть нормальной. У новорожденных и детей первых месяцев жизни на ЭКГ чаще обнаруживают гипертрофию правого желудочка или блокаду правой ножки пучка Гиса, чем гипертрофию левого желудочка.
Рентгенологически можно выявить узурацию нижних краёв рёбер вследствие давления резко расширенных и извитых межрёберных артерий. Сердце может иметь шаровидную или «аортальную», овоидную конфигурацию с приподнятой верхушкой. Рентгенография органов грудной клетки демонстрирует коарктацию в виде знака «3» в области тени верхнего переднего средостения. Размеры сердца нормальные, если только не развивается сердечная недостаточность. Расширенные межреберные коллатеральные артерии могут узурировать 3-8-е ребра, в результате чего на ребрах в области нижнего контура появляются углубления, в то же время узуры ребер редко формируются до 5-летнего возраста.
При сканировании аорты используют супрастернальную позицию. Косвенные эхокардиографические признаки, подтверждающие коарктацию, – постстеноти-ческое расширение аорты, гипертрофия и дилатация желудочков.
Катетеризация сердца и ангиокардиография показаны в случаях, когда не ясен характер сопутствующих пороков сердца или есть подозрение на перерыв дуги аорты.
Дифференциальную диагностику проводят со всеми состояниями, сопровождаемыми повышением артериального давления. В пользу коарктации аорты свидетельствует значительное ослабление или отсутствие пульса на бедренных артериях. Сходные клинические признаки могут быть при неспецифическом аорто-артериите – заболевании аутоиммунной природы, при котором на внутренней оболочке крупных сосудов развивается пролиферативный процесс, в результате чего уменьшается просвет сосудов и повышается артериальное давление. Из-за асимметричного поражения сосудов неспецифический аорто-артериит называют «болезнью разного пульса».
[9], [10], [11], [12], [13], [14], [15]
Лечение коарктации аорты
Лечение оперативное. У детей первых месяцев и лет жизни порок бывает тяжёлым из-за малого количества коллатералей, что делает необходимым раннее проведение хирургического вмешательства. Если течение порока нетяжёлое. то во избежание рекоарктации в месте коррекции операцию лучше отложить до 6-14 лет. Хирургическое лечение заключается в резекции суженного участка аорты и наложении на этот участок синтетической заплаты.
Новорожденным при наличии клинических проявлений необходима стабилизация сердечнолегочных нарушений, которую проводят обычно путем инфузии простагландина Е1 [0,05-0,10 мкг/(кг х мин), затем снижая до наименьших эффективных доз] для того, чтобы открыть артериальный проток. После этого кровь из легочной артерии сможет поступать в нисходящую аорту через проток, улучшая системную перфузию и препятствуя развитию метаболического ацидоза. Короткодействующие инотропные препараты (например, допамин, добутамин), диуретики и О2 применяются для лечения сердечной недостаточности.
До проведения коррекции для лечения гипертензии можно применять блокаторы; следует избегать назначения ингибиторов АПФ. После операции для коррекции гипертензии применяют блокаторы, ингибиторы АПФ или блокаторы рецепторов ангиотензина II.
Дискутабельным является вопрос о предпочтительном методе радикальной коррекции порока. В некоторых центрах предпочитают проводить баллонную ангиопластику с или без стентирования, однако в других предпочитают хирургическую коррекцию и оставляют баллонную ангиопластику для рекоарктации после хирургической коррекции. Начальная частота успешной коррекции после баллонной ангиографии составляет 80-90 %; при последующих катетеризациях можно расширять стент по мере роста ребенка.
Операции для коррекции коарктации включают резекцию и наложение анастомоза конец в конец, аортопластику заплатой и аортопластику лоскутом из левой подключичной артерии. Выбор зависит от анатомии порока и предпочтений центра. Хирургическая летальность составляет менее 5 % при наличии клинических проявлений у грудных детей и менее 1 % у более старших детей. Часто сохраняется остаточная коарктация (6-33 %). Редко развивается параплегия в результате пережатия аорты во время операции.
Все пациенты вне зависимости оттого, была ли проведена коррекция порока или нет, должны получать профилактику эндокардита перед стоматологическими или хирургическими процедурами, при которых возможно развитие бактериемии.
Источник
Клиника коарктации аорты. Диагностика коарктации аорты.
Резкая коарктация аорты проявляется уже на первом месяце жизни как общими, так и специфическими симптомами. Для детей этого возраста характерно повышенное беспокойство, отсутствие аппетита, значительный дефицит массы тела.
Нередко детей долго лечат по поводу пневмонии, и только тщательное обследование позволяет обнаружить порок. Диагностика затрудняется тем, что нет характерной аускультативной картины, на которую обычно опираются врачи при выявлении пороков сердца. Чаще всего имеется лишь небольшой систолический шум слева от грудины, проводящийся в межлопаточную область. Более выраженная шумовая картина возникает при сопутствующем ОАП или ДМЖП, но и она может быть «смазана» в случаях высокого легочного сопротивления у новорожденных. Наиболее легко выявляется такой симптом коарктации аорты, как резкое ослабление пульса на ногах. Точный диагноз можно поставить при сочетании сердечной недостаточности, артериальной гипертензии на верхних конечностях и градиенте систолического давления между правой рукой и ногой.
Наиболее характерный признак порока в этом возрасте – сердечная недостаточность, проявляющаяся прежде всего тахикардией и одышкой. Если не проводится терапевтическое лечение, возникают задержка жидкости, увеличение печени, периферические отеки; в легких выслушиваются влажные мелкопузырчатые хрипы. Основным фактором, предъявляющим повышенные требования к сердцу, служит механическое препятствие кровотоку в аорте. Степень нарушения кровообращения зависит также от наличия коллатералей и быстроты развития компенсаторной гипертрофии сердца. Частота сердечной недостаточности обратно пропорциональна возрасту, в котором впервые проявляется коарктация аорты. В первые три месяца жизни сердечная недостаточность присутствует у 100% больных, среди пациентов 1 года -у 70%, в возрасте от 1 года до 15 лет — у 5% пациентов.
При недостаточно быстрой гипертрофии левого желудочка (у 15— 20% больных) его насосная функция быстро падает, что резко утяжеляет состояние. У таких детей наблюдается выраженная кардиомегалия за счет миогенной дилатации. Тоны сердца приглушены, нередко выслушивается шум митральной недостаточности. В этих случаях сердечная недостаточность быстро прогрессирует, несмотря на интенсивную терапию.
Другим симптомом является изменение артериального давления. Нормальное артериальное давление на первой неделе жизни у здоровых детей составляет 70+9/40±6 мм рт. ст. К концу первого месяца жизни оно равно 90±8/60±9 мм рт. ст. При коарктации аорты систолическое давление на руках значительно возрастает и может превышать 110—120 мм рт. ст. Измерение давления на обеих руках позволяет исключить отхождение одной из подключичных артерий ниже области коарктации. В случае такой аномалии давление на соответствующей руке на 10—30 мм рт. ст. ниже, чем на противоположной.
Сравнительно невысокая артериальная гипертензия (при наличии выраженной коарктации) может встретиться у больных с сопутствующим клапанным стенозом аорты, большим ДМЖП или тяжелой сердечной недостаточностью. Однако по мере лечения последней и увеличения сердечного выброса артериальное давление может возрастать.
Как уже отмечалось, у новорожденных физиологическая узость перешейка аорты создает градиент давления между руками и ногами, который примерно у 16% детей превышает 20 мм рт. ст. Однако, как правило, он быстро снижается в течение нескольких дней. При истинной коарктации градиент давления обычно, наоборот, нарастает, превышая 30 мм рт. ст.
Особое внимание необходимо уделять функции ОАП у новорожденных с предуктальной коарктацией аорты. Закрытие протока у таких детей приводит к острой гипоперфузии нижней половины туловища, молниеносному развитию тяжелой недостаточности кровообращения, нарушению функции почек и быстрой гибели. Неблагоприятным прогностическим признаком у этих пациентов является уровень мочевины в крови более 10 ммоль/л.
– Также рекомендуем “Инструментальные методы при коарктации аорты. Лечение коарктации аорты.”
Оглавление темы “Патология сосудистой системы и сердца.”:
1. Гемодинамика при коарктации аорты. Течение коарктации аорты у ребенка.
2. Клиника коарктации аорты. Диагностика коарктации аорты.
3. Инструментальные методы при коарктации аорты. Лечение коарктации аорты.
4. Перерыв дуги аорты у ребенка. Гемодинамика при атрезии дуги аорты.
5. Диагностика перерыва дуги аорты у новорожденного. Лечение атрезии дуги аорты.
6. Опухоли сердца. Диагностика и признаки опухолей сердца.
7. Рабдомиома сердца. Виды рабдомиом сердца. Признаки рабдомиомы сердца.
8. Клиника опухоли сердца. Лечение и операции при опухолях сердца.
9. Заболевания миокарда воспалительного характера. Диагностика воспаления сердца.
10. Кардиомиопатии. Эпидемиология или распространенность кардиомиопатий.
Источник
Коарктация аорты (КоА) в структуре возможных причин артериальной гипертензии (АГ) у детей занимает не первое место, заметно уступая нефрогенной гипертензии. Частота КоА у детей составляет около 10% всех случаев симптоматической АГ. Однако возможность КоА необходимо иметь в виду у любого ребенка с АГ, поскольку в данном случае причина гипертензии является потенциально устранимой. Хирургическая коррекция этого порока (резекция аорты с наложением анастомоза, установление синтетического протеза или баллонная ангиопластика) позволяет нормализовать артериальное давление и значительно продлевает жизнь больного. В то же время при отсутствии лечения каждый пятый больной умирает до 20 лет, а 80% больных не доживает до 50 лет. При этом ожидаемая продолжительность жизни больного с КоА после хирургического лечения тем больше, чем раньше установлен диагноз и проведено вмешательство.
В типичных случаях диагностика КоА не является сложной задачей при условии, что врач осведомлен о возможных симптомах этого заболевания. Решающее значение в диагностике КоА имеет определение характера пульса на руках и ногах — отсутствие или резкое ослабление пульса на бедренных артериях и напряженный пульс на кубитальных и лучевых артериях. Систолическое АД на ногах ниже, чем на руках; как у здорового, так и у больного с АГ иного генеза соотношение обратное. Систолический шум изгнания лучше всего выслушивается не над областью сердца, а сзади в межлопаточной области слева (место проекции перешейка аорты).
Таким образом, соблюдение несложных правил физикального обследования больного с АГ позволяет врачу заподозрить КоА уже у постели больного. К таким правилам относятся:
- определение пульсации не только на лучевых, но и на бедренных артериях;
- обязательное измерение АД на обеих руках и ногах;
- аускультация не только над областью сердца, но и в межлопаточном пространстве и над областью живота. Приводим историю болезни мальчика с типичными проявлениями КоА.
Пример поздней диагностики КоА.
Олег Т., 13 лет, поступил в МДГКБ для обследования в связи с наличием АГ, причина которой не была установлена. С 8-летнего возраста периодически жаловался на головные боли, повышенную утомляемость. В 11 лет впервые измерено АД и выявлено его повышение. Обследован в стационаре по месту жительства (г. Киев), однако, со слов родителей, причина гипертензии установлена не была.
При поступлении в МДГКБ мальчик жалоб не предъявлял, хотя АД было стойко повышенным (максимально до 150/100 мм рт.ст.). При первом же осмотре обращали на себя внимание такие особенности хабитуса, как чрезмерно развитый плечевой пояс, видимая на глаз усиленная пульсация сонных и аксиллярных артерий. Пульс на лучевых артериях с обеих сторон был напряженным, в то же время на бедренных, подколенных артериях и на сосудах стопы пульсация не определялась. АД на ногах также не определялось. Граница сердца была расширена влево, а при аускультации выслушивался систолический шум с punctum maximum в межлопаточном пространстве слева.
Эти данные позволили прийти к выводу, что АГ у мальчика обусловлена коартацией аорты. Это предположение подтвердилось данными инструментальных исследований: на ЭКГ были выявлены признаки перегрузки левых отделов сердца, на ЭхоКГ — расширение корня аорты. Несмотря на то что эти симптомы являлись только косвенными признаками КоА, имеющихся данных было достаточно для направления больного на консультацию кардиохирургу. Поскольку у кардиохирурга диагноз КоА не вызывал сомнений, пациенту была рекомендована госпитализация в специализированное отделение НИИ хирургии им. А.В. Вишневского для проведения аортографии и оперативного лечения.
В данном случае у подростка отмечалась умеренная АГ, которая могла бы быть и первичной, а характер жалоб был крайне неспецифичным и не позволял склониться в пользу какого-либо определенного диагноза. Однако первое же корректно проведенное физикальное обследование позволило заподозрить КоА благодаря специфическому характеру пульса и характерному соотношению АД на верхних и нижних конечностях. При этом особо следует остановиться на полноте физикального обследования, так как рутинный осмотр без направленного поиска возможных симптомов КоА не позволял в течение нескольких лет установить генез гипертензии, несмотря на проведенное в условиях стационара обследование. Это обусловлено тем, что все данные инструментальных исследований, за исключением ультразвукового допплеровского исследования и аортографии, не выявляют прямых признаков КоА, и этот порок невозможно обнаружить случайно. Подобная неполнота физикального обследования особенно опасна, если у больного с АГ наряду с КоА выявляется какое-либо сопутствующее заболевание, которое также способно быть причиной АГ, например паренхиматозные заболевания почек.
Приводим историю болезни ребенка с сочетанием геморрагического васкулита с поражением почек и КоА.
Артем М., 10 лет, поступил в стационар с жалобами на появление сыпи на голенях, ягодицах и локтевых суставах, боли и отечность в области локтевых, лучезапястных суставов и отеки тыльной стороны кистей рук, схваткообразные боли в животе и учащенный жидкий стул. За 10 дней до появления настоящих жалоб перенес ОРИ.
При поступлении у мальчика отмечалась обильная экссудативно-геморрагическая сыпь на разгибательной поверхности голеней, ягодицах, вокруг локтевых суставов, на ушных раковинах; местами сыпь была сливной с элементами некрозов. Имелись ангионевротические отеки в области лучезапястных и голеностопных суставов. Живот был вздут, отмечался учащенный жидкий стул со слизью и прожилками крови. Таким образом, у ребенка имелась типичная клиническая картина смешанной формы геморрагического васкулита Шенлейна—Геноха (ГВ) с кожным, суставным и абдоминальным синдромом. Отеки отсутствовали, за исключением локальных ангионевротических отеков на тыле кистей рук и в области голеностопных суставов. Границы сердца были смещены на 1 см влево, а АД было повышено до 140/90 мм рт.ст.
По данным лабораторного исследования у мальчика в первом же анализе мочи имелись изменения в виде протеинурии 0,46 г/л и эритроцитурии 20—30 в поле зрения. Через 5 дней эти изменения усугубились: протеинурия увеличилась до 1,9 г/л, эритроциты сплошь в поле зрения, абактериальная лейкоцитурия до 25 в поле зрения. Таким образом, с первых же дней заболевания развилось поражение почек по типу гломерулонефрита. При этом отечный синдром отсутствовал, лабораторных признаков нефротического синдрома не было, а функция почек не была нарушена (креатинин сыворотки 35 мкмоль/л, мочевина 4,3 ммоль/л).
Поскольку диагноз нефрита при геморрагическом васкулите не вызывал никаких сомнений, казалось естественным расценить АГ как один из симптомов гломерулонефрита. Однако при этом недооценили наличие у ребенка не только расширения границ сердца, но и негрубого систолического шума в III межреберье слева от грудины. Кроме того, АГ у больных с нефритом при ГВ, как правило, появляется не в момент манифестации нефрита, а по мере его прогрессирования и снижения функции почек.
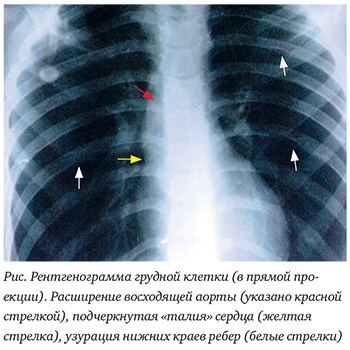 Состояние ребенка длительное время оставалось очень тяжелым главным образом из-за ярко выраженного абдоминального синдрома, который проявлялся сильными болями в животе и тяжелым гемоколитом. Только на 10 день нахождения в отделении было обращено внимание на то, что в межлопаточной области у ребенка выслушивается отчетливый систолический шум. Это заставило усомниться , казалось бы, в очевидном выводе, что АГ у мальчика является симптомом поражения почек, и активно искать возможные симптомы КоА. Выяснилось, что при поступлении в стационар АД было измерено впервые в жизни. При направленном расспросе мать ответила, что ребенок с раннего возраста периодически жаловался на боль в ногах и зябкость ног. Пульс на бедренных артериях был резко ослаблен, АД на ногах было ниже, чем на руках (90/50 мм рт.ст.). Рентгенограмма грудной клетки выявила аортальную конфигурацию сердца с углублением «талии» сердца, расширение корня аорты и узурацию нижней поверхности задних отрезков ребер (рис.).
Состояние ребенка длительное время оставалось очень тяжелым главным образом из-за ярко выраженного абдоминального синдрома, который проявлялся сильными болями в животе и тяжелым гемоколитом. Только на 10 день нахождения в отделении было обращено внимание на то, что в межлопаточной области у ребенка выслушивается отчетливый систолический шум. Это заставило усомниться , казалось бы, в очевидном выводе, что АГ у мальчика является симптомом поражения почек, и активно искать возможные симптомы КоА. Выяснилось, что при поступлении в стационар АД было измерено впервые в жизни. При направленном расспросе мать ответила, что ребенок с раннего возраста периодически жаловался на боль в ногах и зябкость ног. Пульс на бедренных артериях был резко ослаблен, АД на ногах было ниже, чем на руках (90/50 мм рт.ст.). Рентгенограмма грудной клетки выявила аортальную конфигурацию сердца с углублением «талии» сердца, расширение корня аорты и узурацию нижней поверхности задних отрезков ребер (рис.).
Эти данные позволили заподозрить у больного со смешанной формой ГВ коарктацию аорты как сопутствующий диагноз и прийти к выводу, что его АГ обусловлена наличием КоА.
У мальчика отмечалось тяжелое течение ГВ с длительными рецидивами геморрагических высыпаний и ангионевротических отеков, с тяжелым поражением желудочно-кишечного тракта в виде гемоколита, энтерита, гастрита. На этом фоне дважды (через месяц и через 3 мес после дебюта заболевания) отмечалось развитие перитонита вследствие перфорации язвы поперечно-ободочной кишки. Не исключено, что именно наличие КоА, т.е. нарушение кровоснабжения не только почек и нижних конечностей, но и кишечника, послужило предрасполагающим фактором к развитию этого редкого для геморрагического васкулита осложнения. О роли КоА в развитии изъязвления кишечника косвенно свидетельствует тот факт, что повторное прободение произошло уже в период, когда прекратились рецидивы высыпаний, нормализовался стул и прекратились боли в животе.
Через год после дебюта ГВ, когда контрольное обследование констатировало ремиссию нефрита, ребенок был госпитализирован в Институт хирургии им. А.В. Вишневского, где диагноз КоА подтвержден при проведении аортографии и проведена оперативная коррекция порока.
Таким образом, в данном случае наличие паренхиматозного заболевания почек привело, во-первых, к тому, что не были замечены и соответственно были недооценены физикальные изменения со стороны сердечно-сосудистой системы. Во-вторых, кажущаяся очевидность нефрогенной природы гипертензии привела к тому, что не было обращено внимание на то, что АД у ребенка ранее никогда не измерялось, и потому гипертензия могла оказаться не острой, а хронической. Тщательный сбор анамнеза и установление времени возникновения АГ, а также жалоб и симптомов, сопутствующих ее появлению, нередко недооценивается, что приводит к ошибкам в трактовке ее симптомов у больных с сочетанием двух заболеваний, каждое из которых теоретически может быть причиной подъема АД.
Иллюстрацией сочетанного поражения сердца и почек может служить и следующее наблюдение.
Мальчик, 7 лет, был доставлен в МДГКБ с диагнозом «коарктация аорты. Гипертонический криз». Причиной обращения к врачу были остро возникшие жалобы на головную боль, тошноту и недомогание; АД при осмотре оказалось повышенным (150/90 мм рт.ст.). Поскольку мальчик в 2-летнем возрасте был оперирован по поводу КоА, АГ связали именно с этим заболеванием. При этом недооценены были анамнестические данные о том, что ребенок наблюдался кардиохирургом, ему регулярно измерялось АД и оно было нормальным всего за несколько месяцев до настоящего заболевания. Таким образом, речь не могла идти о резидуальной гипертензии у больного с остаточной обструкцией после хирургической коррекции КоА. После того как в МДГКБ был уточнен анамнез и было установлено, что АГ развилась остро, диагностический поиск был направлен на другие заболевания, которые могли бы быть причиной остро развившейся АГ, и в первую очередь на заболевания почек. При сборе анамнеза выяснилось, что появлению настоящих жалоб предшествовал перенесенный около 2 нед назад фарингит, а тщательный осмотр выявил наличие небольших плотных отеков на веках, голенях и передней брюшной стенке, что заставило предположить острый постстрептококковый гломерулонефрит. Диагноз был подтвержден наличием типичного мочевого синдрома (протеинурия до 0,4 г/л, эритроцитурия до 50—60 в поле зрения и абактериальная лейкоцитурия 10—12 в поле зрения), повышением титра АСЛ:О и быстрой нормализацией АД на фоне бессолевой диеты и диуретической терапии.
Данные примеры показывают, что для правильной трактовки такого симптома, как АГ, недостаточно установить наличие заболевания, одним из симптомов которого является повышение АД. Необходимо также установить, имеет ли АГ у данного пациента ряд особенностей, характерных именно для предполагаемого заболевания. Такие несложные действия, как правильный сбор анамнеза относительно предшествующих измерений АД и полноценное физикальное обследование, помогают избежать диагностических ошибок в случаях сочетания у больного двух заболеваний.
- Белоконь Н.А., Кубергер М.Б. Болезни сердца и сосудов у детей. Руководство для врачей: в 2 т. Т. 1. М.,1987. 448 с.
- Брязгунов И.П. Симптоматические артериальные гипертензии в практике педиатра. М., 2003. 112с.
- Вербовская Н.В., Гринштейн Ю.И. Артериальная гипертония у больных с коарктацией аорты. Осо- бенности функциональной диагностики и клинической картины. Сибирское мед. обозрение, 2008;52(4):64—67.
- Педиатрия: национальное руководство: в 2 т. М., 2009;2: 1024 с.
- Мутафьян О.А. Артериальные гипертензии и гипотензии у детей и подростков (клиника, диагностика, лечение).СПб.: Невский Диалект; М., 2002. 144 с.
- Кардиология и ревматология детского возраста / под ред. Самсыгиной Г.А., Щербаковой М.Ю. М., 2004.744 с.
Источник
